बेंगलुरु : इंडियन इंस्टीट्यूट ऑफ साइंस (IISc) के शोधकर्ताओं की एक अंतःविषय टीम ने कैंसर कोशिकाओं के माइक्रोएन्वायरमेंट की जांच के लिए एक 3-डी ट्यूमर मॉडल और चुंबकीय रूप से संचालित नैनोमोटर्स का उपयोग किया है. इस टीम में सेंटर फॉर नैनो साइंस और इंजीनियरिंग (CeNSE) और आणविक प्रजनन, विकास और आनुवंशिकी विभाग (MRDG) के केंद्र के शोधकर्ता शामिल हैं.
अंगेवंडे चेमी में प्रकाशित इनके काम में टीम ने ट्यूमर मॉडल से बाहरी चुंबकीय क्षेत्र के माध्यम से दूरस्थ रूप से पेचदार नैनोमोटर्स को दूर किया, जो सेलुलर वातावरण में परिवर्तन, नक्शा और मात्रा निर्धारित करता है. मॉडल में एक पुनर्गठित बेसमेंट झिल्ली मैट्रिक्स के भीतर एम्बेडेड दोनों स्वस्थ और कैंसर कोशिकाएं शामिल हैं, जो स्तन कैंसर के वातावरण की नकल करती है.
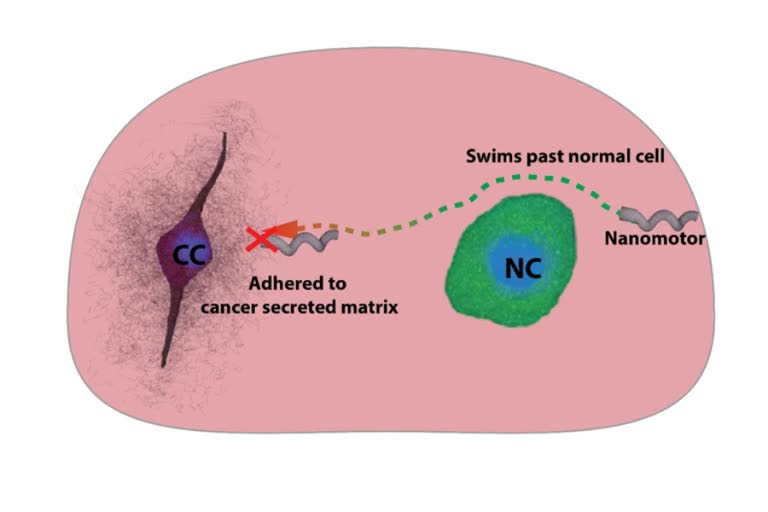
यह अध्ययन ट्यूमर के अंदर बढ़ने वाली कैंसर कोशिकाओं को लक्षित करने के एक नए तरीके पर प्रकाश डालता है और कैंसर की जगह के आसपास के क्षेत्र में स्थानीयकरण करने के लिए उनका इंतजार करता है. सीएनएसईई के सह-प्रथम लेखक और पीएचडी छात्र देबायन दासगुप्ता कहते हैं कि हमने एक ट्यूमर मॉडल में कैंसर कोशिकाओं की ओर नैनोमोटर्स को चलाने की कोशिश की और उन्हें कैंसर कोशिकाओं के पास मैट्रिक्स से चिपकते हुए देखा, लेकिन ऐसा सामान्य कोशिकाओं के पास नहीं हुआ.
बाह्य मैट्रिक्स (ईसीएम) प्रोटीन और कार्बोहाइड्रेट का एक जटिल 3 डी नेटवर्क है, जो जीवित कोशिकाओं द्वारा उनके पड़ोस में निकलता है. हालांकि जब कैंसर कोशिकाएं ईसीएम में ताजी सामग्री (मेटेरियल) का स्राव करती हैं, तो यह स्थानीय वातावरण को खराब करते हुए स्वस्थ कोशिकाओं के आसपास के देशी ईसीएम की रासायनिक और भौतिक संरचना को बाधित करता है. इसलिए हमेंं यह समझना कि कैंसर कोशिकाओं के कारण सेलुलर माइक्रोएन्वायरमेंट कैसे बदल जाता है और इन परिवर्तनों को मापना मात्रात्मक रूप से कैंसर की प्रगति को समझने में महत्वपूर्ण हो सकता है.
वर्तमान अध्ययन में शोधकर्ताओं ने पाया कि जैसे ही नैनोमोटर्स कैंसर कोशिका झिल्ली के पास पहुंचते हैं वह सामान्य कोशिकाओं की तुलना में अधिक मजबूती से मैट्रिक्स से चिपक जाते हैं. मैट्रिक्स से बंधे नैनोमोटर्स कि दृढ़ता से मापने के लिए टीम ने चिपकने वाली ताकत को दूर करने और आगे बढ़ने के लिए आवश्यक चुंबकीय क्षेत्र की ताकत की गणना की.
इसका मतलब है कि कैंसर कोशिकाएं कुछ कर रही हैं. इसलिए हमने कुछ माप किए और यह पता लगाया कि यह (चिपकने वाला बल) कोशिकाओं के प्रकार पर निर्भर करता है. बातचीत की ताकत और यह भी कि नैनोमीटर किस सेल के पास पहुंचता है. सेंटर फॉर नैनो साइंस और इंजीनियरिंग के एसोसिएट प्रोफेसर और वरिष्ठ लेखक अंबरीश घोष बताते हैं कि अंत में हमने वास्तव में एक महत्वपूर्ण जैविक वातावरण की भौतिक संपत्ति की खोज की.
नैनोमोटर्स कैंसर कोशिकाओं को अधिक चिपकाने का कारण उनके आरोपित ईसीएम हैं. शोधकर्ताओं ने पाया कि यह 2,3-लिंक्ड सियालिक एसिड एक शर्करा -संयुग्मित अणु की उपस्थिति के कारण हो सकता है, जो कैंसर कोशिकाओं के वातावरण पर नकारात्मक चार्ज डालता है. उन्होंने फ्लोरोसेंट मार्करों का उपयोग करके इन शर्करा के वितरण की कल्पना की और पाया कि सियालिक एसिड कैंसर कोशिका की सतह से 40 माइक्रोमीटर तक वितरित किए गए थे और उसी दूरी पर थे, जब तक कि नैनोमोटर्स ने मजबूत आसंजन का अनुभव नहीं हुआ.
इस चिपकने वाले प्रभाव का मुकाबला करने के लिए टीम ने नैनोमोटर्स को पेरफ्लुओरोक्यूलेटाइलथ्रीओक्सिसिलीन (पीएफओ) के साथ लेपित किया, जिसने उन्हें चार्ज किए गए वातावरण से ढाल दिया. लेपित नैनोमोटर्स कैंसर कोशिकाओं के पास मैट्रिक्स से चिपके नहीं थे, जबकि अनकोटेड मोटर्स मैट्रिक्स से चिपके हुए थे. यह इस तथ्य की पुष्टि करते है कि नकारात्मक चार्ज किए गए कैंसर माइक्रोनिनिटर्स आने वाले नैनोमोटर्स के साथ जुड़ते हैं और उन्हें इम्मोनियल प्रदान करते हैं.
एमआरडीजी में सहायक प्रोफेसर और वरिष्ठ लेखकों में से एक राम्रे भट ने कहा कि यह जानकर हैरानी होती है कि इस तरह के एक बड़ी जॉच से हमने पाया कि आक्रामक कैंसर कोशिकाओं ने विशेष रूप से चार्ज किए गए शर्करा को चिपचिपा और समृद्ध बनाकर अपने परिवेश को फिर से तैयार किया. यह चार्जिंग संभवतः उनके सामान्य समकक्षों के बीच छिपी हुई कैंसर कोशिकाओं की छोटी आबादी को लक्षित करने और मारने के लिए इस्तेमाल किया जा सकता है, जिसके लिए हम इन अध्ययनों को जीवित जानवरों तक पहुंचा रहे हैं.